预先定义的药品质量目标是什么?
配方与工艺的相互关系调整会对药品关键属性产生何种影响?
是否能回答上述问题?如果可以,那么你的答案来自哪里?来自研发工作研究得出的实验数据、以及文献上的知识吗?是依据质量源于设计的原则吗?
质量源于设计的一个关键元素就是“设计空间”的概念,其是能保证产品合理性能属性的一个由产品设计和工艺变量构成多维空间。产品和工艺的变更只要不出这个空间,那么变更实施无需再批准。听上去“设计空间”的概念很美丽,但现实却很骨感,在实际研发、放大及规模商业化生产上,我们的科研人员和工程师遇到了很大的挑战。
作者在文章中介绍如何将“设计空间”的概念在冻干工艺在研发、放大及转移上进行应用。
1995 Chang 和Fischer 提出过一个确定冻干工艺设计空间的想法,如下图
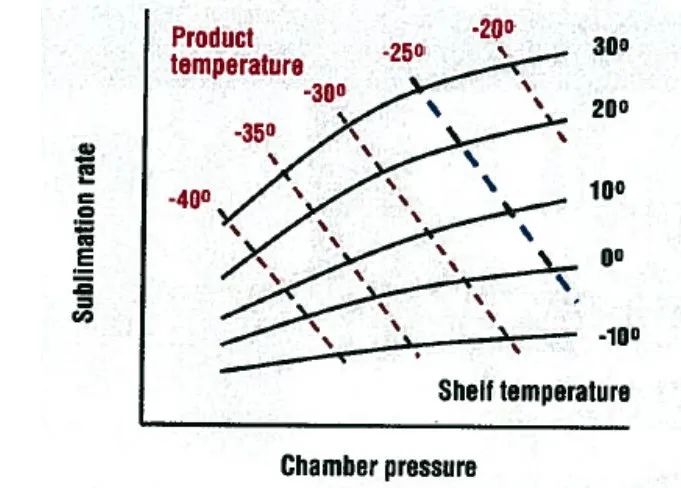
图一
升华速率为X轴,Y轴体现箱体压力,从而对产品温度、板层入口温度及箱体压力之间的关系进行描述。要知道,箱体压力对产品温度和升华速率是有很复杂的影响:
1. 较高的箱体压力将降低水汽从产品升华到箱体内的驱动力。这个驱动力可定义为产品冰界面内压力与箱体压力的压力差(Pi-Pc)。从图1中,可以看出,一定温度的产品其升华速率随箱体压力的增加而线性降低。
2. 较高的箱体压力将增加热传导率,也就是提高瓶底与板层之间细小缝隙中的气体的热传导性。这种影响将会增加产品温度,这会带来产品冰内的气体压力的升高,从而提高冰界面内的水汽压力。不难理解水汽升华至箱体内的驱动力也就提高了。
可见,较高箱体压力最直接的作用是提高产品温度和产品的升华速率,但需要意识到,这种作用所带来的热传导能力的提高比升华速率的提高更具负面意义。因此,有效工艺是期望将初次干燥过程中的产品目标温度能在最高的板层温度和最低的箱体压力间进行维持。
怎么测量升华速率
最传统的方式是称重测量。即冻干周期开始前,称量一定量西林瓶的重量Wi,初次干燥完成后,再称量Wp,然后用干燥时间t,计算平均升华速率(Wi-Wp)/ t。很显然,这是一种破坏性试验。
现在有一种过程分析技术应用于冻干工艺,即之前提到的TDLAS—— Tunable diode laser absorption spectroscopy 可调谐半导体激光吸收光谱技术,此装置安装于冻干箱体和冷阱之间的连接管(主阀区)上。基本原理是让近红外光束(near- infra red beam)与箱阱连接通路轴线成一定夹角,水的吸收波段多普勒频移被测量,两吸收峰值的频移比例换算为水汽通过的速度。由于通径已知,且水汽浓度也可以通过传统吸收光谱法测出,从而得出瞬时水汽质量流量。
确定设计空间的边界
1. 定义产品失败模式
通常开发冻干周期是通过对一系列工艺条件(板层温度、箱体压力和时间)的组合进行产品生产试错。常规设计上下限是围绕板层温度、箱体压力和时间而制定的。但在质量源于设计的构想下,研发者必须对能生产出可接受产品的工艺条件图有更深入的理解,通过对试验批的极限条件进行挑战,直到不合格产品产生来,来获得这种理解。
最常见的产品失败是由于冻干崩解。崩解多源于初次干燥时超出产品温度上限(崩解温度),已干燥的部分与粘稠流体混合,从而失去了预冻时形成的微观结构。崩解是不可接受的现象,其会导致高水分残留和很差结构属性。对于大多数配方,初次干燥的产品温度上限是共晶点溶解温度。
2. 定义设计空间内的产品实施边界
初次干燥时的产品温度上限取决于配方属性,我们可以通过低温分析仪器和冻干显微镜来获得。举例,假设某配方产品,初次干燥时的产品温度上限为-25度,我们将其在图一中以虚线标出(见下面的图2),定义为产品配方属性所决定的设计空间实施边界。
3. 定义设计空间内的设备实施边界
通常情况,研发、中试和规模生产各自所用的设备使用者不是同一拨人,因此彼此并不了解和关心设备间的差异。比如,研发人员用实验室型设备进行冻干周期开发,但他们并不考虑中试设备性能的限度;当冻干配方转移到临床样品生产的公司后,会发现冻干周期并不能生产出合格产品,导致项目的延期。此现象很常见吧?这说明在周期开发时,我们就应将将来生产型设备的能力限度考虑进去。
设备能力的限度有很多种可能因素构成,比如箱阱通径不一样、冷阱制冷能力不同、冷阱冷凝面积不一样, 循环系统加热功率不同,板层热损失或传热系数不同…
设备的性能限度不同会有不同的“最大”升华速率,因此其构成了设计空间内的一个水平上边界。
这里还有一个更复杂的冻干机性能限度,这就是通过箱阱之间通路的汽流动力学。汽流的产生是由于箱阱间的压差所引起的,通常越高的压差带来越快的水汽通过连接管路的流速。恒定水汽的质量流量通过管路,速度会加快,从而导致箱阱间的压差持续降低。但热力学显示,这个速度的限度与水汽气中的声速(400m/s, 1马赫)相对应,当水汽速度接近1马赫,水汽流量将会被阻塞,下游压力再下降也不会影响通过管路的质量流量。冻干过程中,一旦流量被阻,将会导致冻干箱体内的压力失控。
与其它设备性能限度不同,由于气流阻塞所带来的能力限度与系统压力有关,质量流量的阻塞点(chokepoint)与压力成直接比例关系,此边界在设计空间上的大概形态以实线在图中标出。
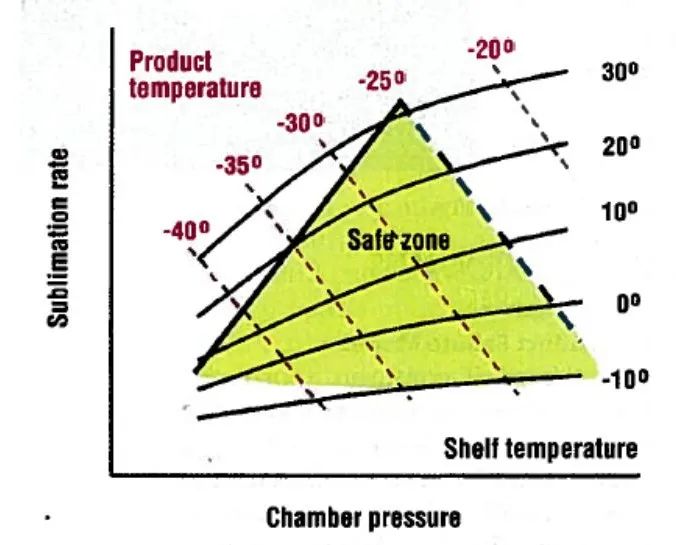
图二
因此,以这个产品为例,设计空间由右侧的产品边界和左侧气流阻碍边界(设备)构成,任何空间内的工艺条件都应可接受,当然,空间顶点区域附近是最有效的工艺条件。
进行一系列冻干机捕冰能力测试是很好的验证设备能力限度的方式。在设定的压力下,对板层线性斜率升温,在某时刻,箱体控制压力失控,这就是与阻塞点有关。为了评估此设备在此设定压力下所能支持的升华速率,需要不断测试,找到正确的压力与板层温度的关系,直到初始冰量的很大一部分已经被升华。然后再设定一个新的压力控制点进行测试,直到收集足够的数据能绘出图中的阻碍点线。
当然,TDLAS可以有效减少此设备能力验证的工作量,理论讲其可以在一次捕冰实验中确定出阻碍点曲线。
此外,检测设备在捕冰测试中其它能力也是有必要的,比如检测冷阱温度是否维持在特定温度下,如-50. 这些设备能力限度会体显为设计空间的水平线。
最后,要生成一个像文中提及的设计空间,需要对配方和设备有深入的理解,这也是QbD质量原因设计所追求的。
此文翻译摘抄自 Steven L. Nail, Jim A. Searles, 2008年 在 International BioPharm 上发表的 Elements of Quality by Design in Development and Scale-up of Freeze- Dried Parenterals
1
本文来源于拾西,由“制药业”平台整理发布,仅供交流学习,转载请注明出处。欢迎关注“制药业”公众号,获得最新制药业创新技术、新闻动态等热点话题。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..